BioNTech und Pfizer: Teilerfolg für COVID-19 Impfstoff Comirnaty in den USA - Druck auf Moderna
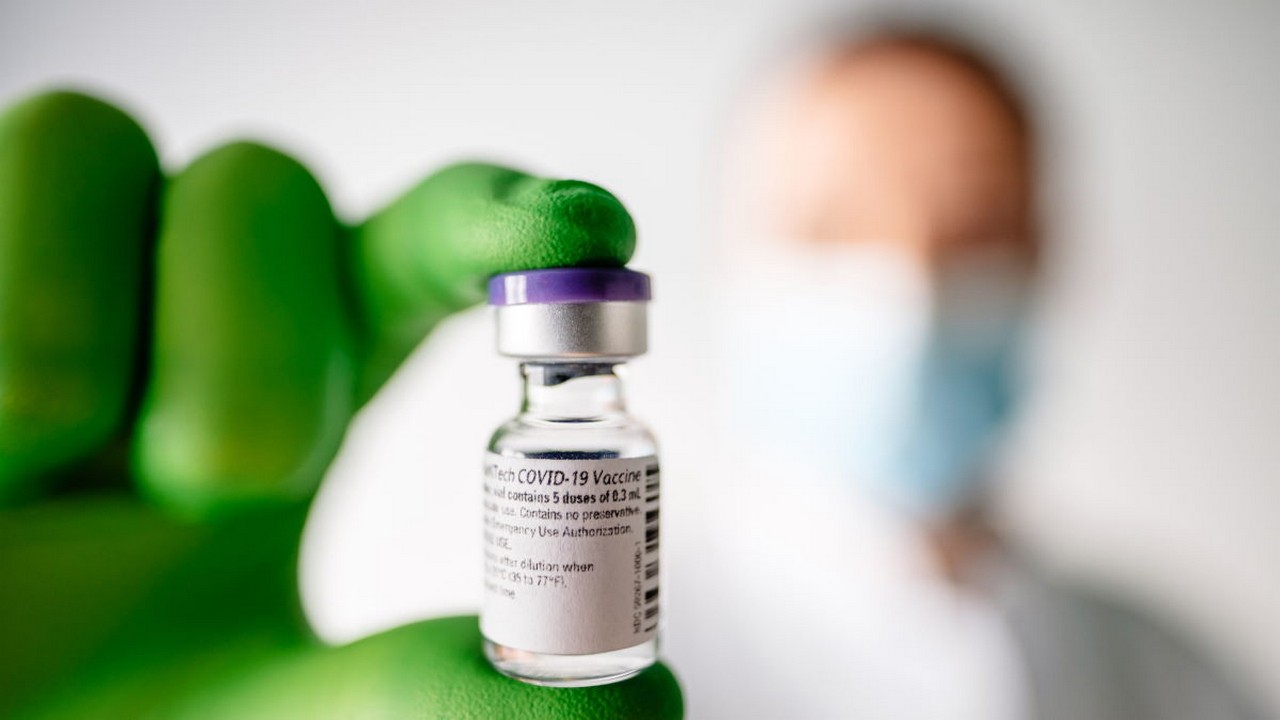
Mit Spannung war an der Börse ein Beratungstermin bei der FDA zum Thema Booster-Impfungen mit dem COVID-19 Impfstoff Comirnaty von BioNTech und Pfizer für die US-Bürger erwartet worden. Am Ende kam es wie von vielen erwartet: Einem Antrag der beiden Unternehmen, Booster-Impfungen für alle Personen ab 16 Jahren zu empfehlen, erteilte der Beratungsausschuss für Impfstoffe und verwandte biologische Produkte der US-Zulassungsbehörde eine Absage.
Anders sieht dies bei Personen aus, die 65 Jahre und älter sind oder einem hohem Risiko für einen schweren COVID-19-Krankheitsverlauf ausgesetzt sind. Diese sollen in einem Abstand von sechs Monaten nach der letzten Impfung eine Auffrischungsimpfung mit Comirnaty erhalten können. Zudem sollen auch Personen aus dem Gesundheitswesen und anderen Berufen mit hohem Kontaktrisiko einen solchen Booster erhalten können.
Mit der Empfehlung des Beraterausschusses ist noch keine endgültige Entscheidung der FDA über die Notfallzulassung einer Auffrischungsimpfung mit Comirnaty getroffen worden. Diese wird in den kommenden Tagen erwartet. Experten gehen davon aus, dass die FDA sich der Meinung des Beraterausschusses anschließen wird. In den kommenden Tagen wird auch noch die US-Behörde CDC über Booster beraten.
Diskussionen gab es im Ausschuss vor allem um potenzielle Nebenwirkungen und die Effizienz des Impfstoffs. Booster-Impfungen sind aktuell umstritten, unter anderem da in Teilen der Welt Impfstoffe gegen COVID-19 weiter Mangelware sind und entsprechend niedrige Impfquoten vorhanden sind. Details zum Verlauf des Hearings im FDA Beraterausschuss hat unter anderem die US-Journalistin Meg Tirrell in einem umfangreichen Thread auf Twitter veröffentlicht.
BioNTech und Pfizer wollen weiter auf umfangreichere Zulassungen für Booster-Impfungen hinarbeiten
„Wir sind entschlossen, die laufenden Bemühungen zur Reduzierung von Infektionen und COVID-19-Fällen zu unterstützen. Die Daten, die wir der FDA, der Europäischen Arzneimittel-Agentur (EMA) und anderen Aufsichtsbehörden vorgelegt haben, unterstreichen, dass eine Auffrischungsimpfung eine starke Immunreaktion gegen alle getesteten Varianten hervorruft und dazu beitragen könnte, dringende Bedürfnisse der öffentlichen Gesundheit zu adressieren“, sagt Özlem Türeci, Chief Medical Officer und Mitgründerin von BioNTech.
Das Mainzer Unternehmen hat damit einen Vorsprung beim Thema Booster in den USA gegenüber dem mRNA-Konkurrenten Moderna, dessen Marktwert mit 177,9 Milliarden Dollar an der NASDAQ dagegen - nicht unbedingt berechtigt - weit über den 90,3 Milliarden Dollar von BioNTech liegt - ein Missverhältnis.
Das Thema Booster-Impfungen dürfte nicht nur in den USA, sondern auch in Europa und anderen Regionen auf dem Tisch bleiben - erst recht mit einer steigenden Zahl vorliegender Daten zu den Impfstoffen, die mehr Klarheit über mögliche Risiken und Nebenwirkungen einer dritten Impfdosis bringen werden. Zudem haben Pfizer und BioNTech unter anderem mit Blick auf die Delta-Variante des COVID-19-Erregers angekündigt, weiter auf eine Notfallzulassung von Comirnaty für die gesamte Bevölkerung ab 16 Jahren hinzuwirken.
Hinweis auf Interessenskonflikt(e): Der / die Autor(in) oder andere Personen aus der 4investors-Redaktion halten unmittelbar Positionen in Finanzinstrumenten / Derivate auf Finanzinstrumente von Unternehmen, die in diesem Beitrag thematisiert werden und deren Kurse durch die Berichterstattung beeinflusst werden könnten: BioNTech.




 News
News