Paion reicht erweiterten Antrag bei der EMA ein
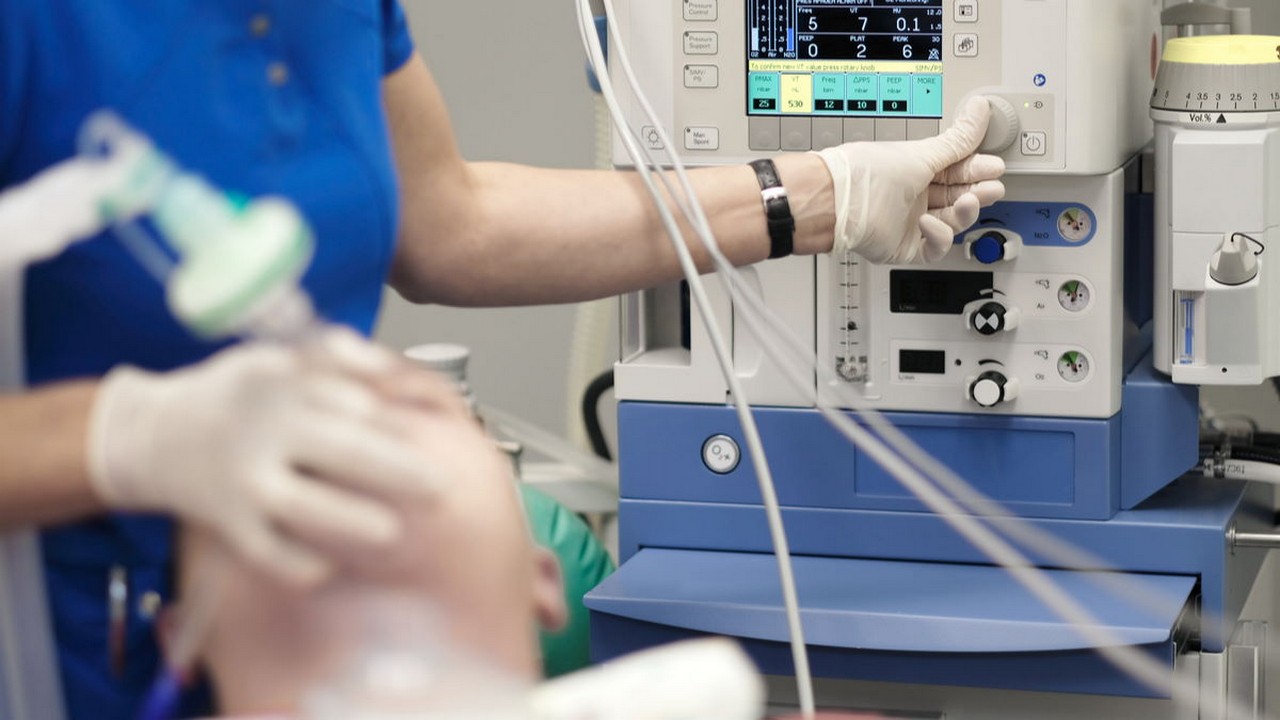
Paion strebt in der Europäischen Union eine Erweiterung der Marktzulassung für Remimazolam an. Einen entsprechenden Antrag hat man bei der Europäischen Arzneimittelagentur (EMA) auf den Weg gebracht.
Schon im März 2021 hatte Paion die Zulassung von Remimazolam zur Kurzsedierung erhalten. Der erweiterte Antrag gilt der Zulassung von Remimazolam für die Allgemeinanästhesie. Der Antrag basiert auf den Ergebnissen einer Phase-III-Studie zu Remimazolam.
Paion erwartet, dass die EMA über den Antrag Ende 2022 oder Anfang 2023 entscheiden wird.
Für Jim Phillips, Vorstandschef von Paion, ist der erweiterte Antrag ein wichtiger Meilenstein für die Erweiterung des europäischen Produktportfolios. Er sieht einen höheren Bedarf für Anästhetika bei komplexen Operationen und Hochrisikopatienten.
Phillips ergänzt: „Remimazolam wurde in Japan und Südkorea bereits für die Allgemeinanästhesie zugelassen. Wir freuen uns nun auf eine gute Zusammenarbeit mit der EMA während des Überprüfungsprozesses mit dem Ziel, Remimazolam auch in dieser Indikation den Patienten in Europa so schnell wie möglich zur Verfügung zu stellen.“




 News
News