Paion - News aus den USA: Remimazolam-Vertrieb startet noch 2020
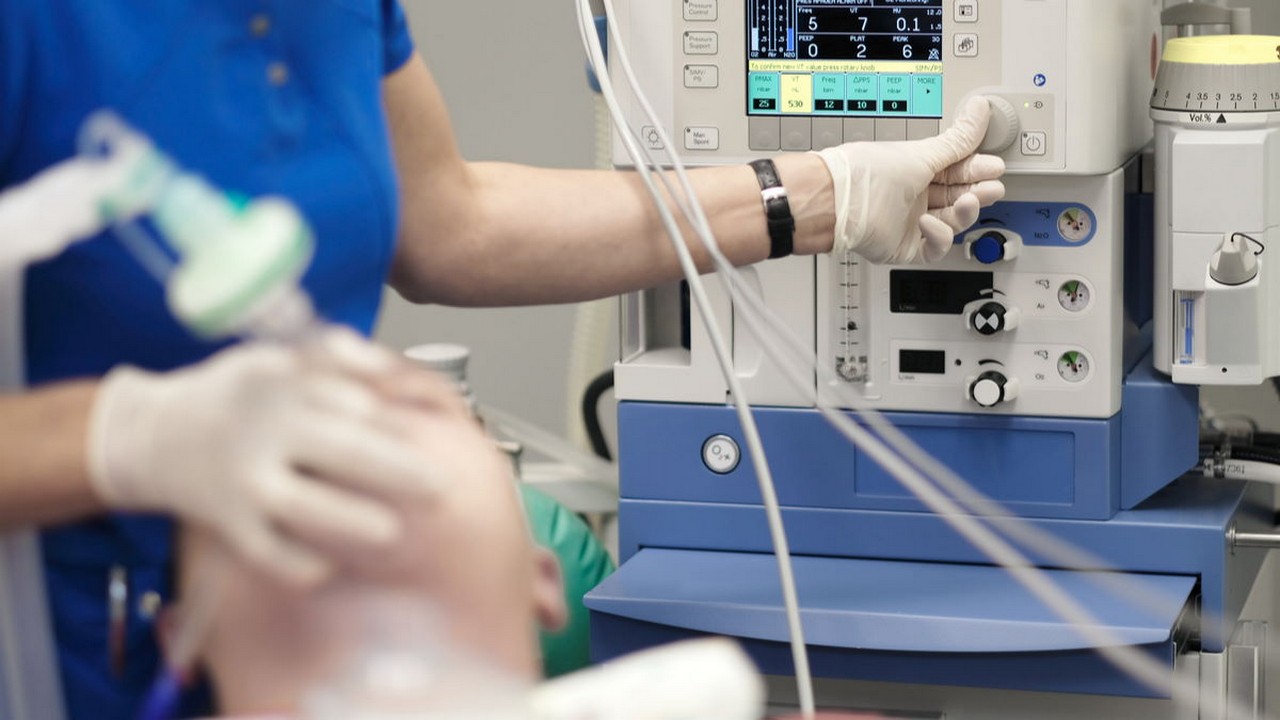
Paion und die US-Partner des Aachener Unternehmens kommen beim geplanten zeitnahen Vermarktungsstart für das neu zugelassene Narkosemittel Remimazolam in den USA entscheidend voran. Von der Drug Enforcement Administration wurde der Wirkstoff als Arzneimittel der Gruppe IV klassifiziert. „In dieser Gruppe sind Arzneimittel mit geringem Missbrauchspotenzial und geringem Abhängigkeitsrisiko eingeordnet. Damit hat BYFAVO die gleiche Eingruppierung erhalten wie z. B. Midazolam und Diazepam”, so Paion am späten Dienstagnachmittag in einer Mitteilung.
Mit der Einstufung der Substanz durch die Drug Enforcement Administration ist eine letzte regulatorische Hürde aus dem Weg geräumt worden. Die FDA hatte im Sommer bereits grünes Licht für Paions Narkosemittel gegeben. Damit steht einem Start der Vermarktung, die noch 2020 beginnen soll, nichts mehr im Wege.
„Wir werden nun mit dem Etikettieren und Verpacken des kommerziellen Produkts beginnen, damit wir BYFAVO den Patienten so schnell wie möglich zur Verfügung stellen können. Wir erwarten, dass das Produkt vor Ende des Jahres in den USA zum Verkauf verfügbar sein wird. Unser erstes Produkt, BARHEMSYS (Amisulprid-Injektion) gegen postoperative Übelkeit und Erbrechen, wurde im August auf den Markt gebracht und wir registrieren bereits Produktverkäufe. Wir freuen uns, diese beiden Medikamente Ärzten und ihren Patienten in den USA anbieten zu können”, sagt Mike Bolinder, CEO von Paions US-Vermarktungspartner Acacia Pharma.

 Diese News zu Paion könnte Sie auch interessieren:
Diese News zu Paion könnte Sie auch interessieren:


 News
News
